
Acquario
La temperatura in acquario è….
..un parametro da non sottovalutare.
La temperatura dell’acqua influisce su quasi tutti gli altri parametri di qualità dell’acqua. È un fattore importante da considerare quando si vuole ottenere una buona qualità dell’acqua. Oltre ai classici effetti di aumento o decremento dello scambio termico, influenza molti altri parametri e può alterare le proprietà fisiche e chimiche dell’acqua.
A questo proposito, la temperatura dell’acqua dovrebbe essere presa in considerazione quando si determina:
- Velocità metaboliche e produzione di fotosintesi
- Tossicità dei composti
- Concentrazioni di ossigeno disciolto e altri gas disciolti
- Conducibilità e salinità
- Potenziale di riduzione dell’ossidazione (ORP)
- pH
- Densità dell’acqua
La temperatura ottimale per la crescita dei batteri nitrificanti, secondo la letteratura, è compresa tra 28°C e 36°C, sebbene per Nitrobacter sia stata riportata da Painter (1970) una temperatura ottimale fino a 42°C. Le costanti di crescita dei batteri nitrificanti sono fortemente influenzate dalla temperatura. La Figura 1, mostra che il tasso di nitrificazione è una funzione di temperature comprese tra 5° e 45° C. Il tasso di crescita massimo si verifica a circa 30° C. La curva A, prodotta da Borchardt (1966) indica che nessuna temperatura ottimale netta può essere definita e che vi è un plateau di attività massima tra 15°C e 35°C. Al di sotto dei 15°C, tuttavia, il tasso di nitrificazione diminuisce drasticamente e si riduce del 50% a 12°C. Wild et al. (1971) trovarono (curva B) che esiste una relazione quasi rettilinea tra il tasso di nitrificazione e la temperatura. Analoghe dipendenze dalla temperatura sono state riportate in schemi di nitrificazione-denitrificazione a stadio singolo. Sono inoltre disponibili dati sugli effetti della temperatura sull’ossidazione dell’ammoniaca in nitrito da parte di Nitrosomonas (curve E, F, G e H) e di nitrito in nitrato da parte di Nitrobacter (curve C e D). Entrambe le specie sembrano essere influenzate in modo simile dalla temperatura. Randall e Buth (1970), tuttavia, hanno dimostrato che sebbene sia la formazione di nitriti che di nitrati fosse fortemente inibita a temperature di 10° C o meno, l’effetto inibitorio dell’abbassamento della temperatura era maggiore per Nitrobacter che per Nitrosomonas; questo era evidente dall’accumulo di nitriti a basse temperature. Barrit (1933) ha scoperto che il punto di morte termica di una coltura pura di Nitrosomonas era compreso tra 54° e 58° C. Quasi nessuna crescita di batteri nitrificanti è stata trovata al di sotto dei 4° C. Le colture di crescita sospese sono più sensibili ai cambiamenti di temperatura rispetto ai biofilm (Murphy e Dawson 1972).
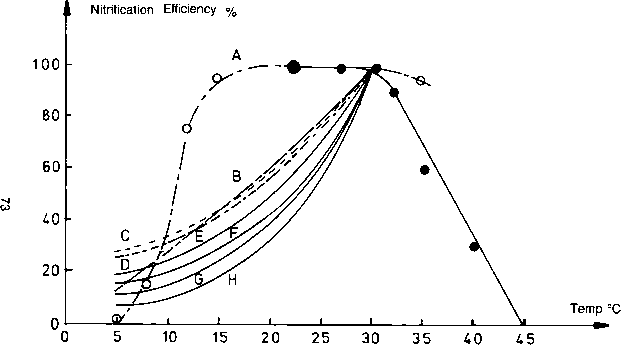
Fig. 1. L’influenza della temperatura sul processo di nitrificazione, presentata nel testo come da A ad H, (Fonte: EPA 1975).
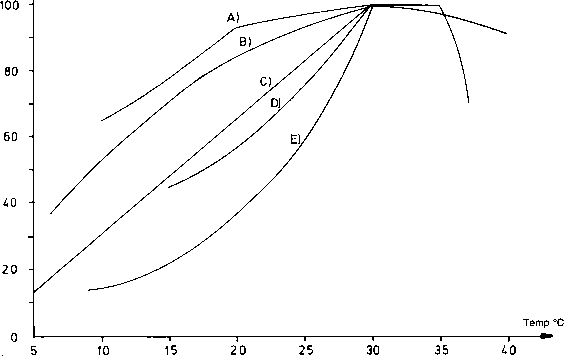
Fig. 2. Confronto sull’effetto della temperatura sulla crescita sospesa (in sospensione) e sui sistemi di nitrificazione della crescita attaccata (biofilm).
Da A) a 0) sono associati sistemi di crescita ed E) è un sistema di crescita sospeso (Fonte EPA 1975).
Temperatura dell’acqua e vita acquatica
Considerata da sola, la temperatura dell’acqua può influenzare i tassi metabolici e l’attività biologica degli organismi acquatici. In quanto tale, influenza gli habitat scelti di una varietà di vita acquatica. Alcuni organismi, in particolare le piante acquatiche, prosperano a temperature più calde, mentre alcuni pesci come le carpe koi o i pesci rossi preferiscono ambienti più freddi.
Gli studi hanno dimostrato una relazione diretta tra i tassi metabolici e la temperatura dell’acqua. Ciò si verifica poiché molti enzimi cellulari sono più attivi a temperature più elevate. Per la maggior parte dei pesci, un aumento di 10°C della temperatura dell’acqua raddoppierà approssimativamente il tasso della funzione fisiologica. Questo aumento del tasso metabolico può essere gestito da alcune specie meglio di altre. L’aumento della funzione metabolica può essere notato nella frequenza respiratoria e nelle risposte digestive nella maggior parte delle specie. L’aumento della frequenza respiratoria a temperature più elevate porta a un maggiore consumo di ossigeno, che può essere dannoso se le frequenze rimangono aumentate per un periodo di tempo prolungato. Inoltre, temperature superiori a 35°C possono iniziare a denaturare, o scomporre, gli enzimi, riducendo la funzione metabolica.
Le fluttuazioni di temperatura possono anche influenzare le scelte comportamentali degli organismi acquatici, come spostarsi in acque più calde o più fredde dopo l’alimentazione, le risposte predatore-preda e le routine di riposo o migrazione.
La temperatura influenza i tassi fotosintetici di diverse alghe
Anche le piante sono influenzate dalla temperatura dell’acqua. Mentre alcune piante acquatiche tollerano acque più fredde, la maggior parte preferisce temperature più calde. Le piante tropicali in particolare mostreranno una crescita e una dormienza limitate a temperature dell’acqua inferiori a 21°C 17. Sebbene la dormienza sia appropriata per sopravvivere a un inverno freddo, per la maggior parte delle piante sono richieste temperature più calde per fiorire.
La temperatura può anche inibire la respirazione delle piante e la fotosintesi. In generale, la fotosintesi delle alghe aumenterà con la temperatura, sebbene specie diverse avranno temperature di picco diverse per un’attività fotosintetica ottimale, al di sopra e al di sotto di questa temperatura, la fotosintesi sarà ridotta.
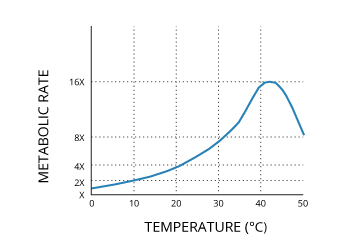
I tassi metabolici degli organismi acquatici aumentano all’aumentare della temperatura dell’acqua.
La temperatura dell’acqua può svolgere un ruolo nel passaggio tra ammonio e ammoniaca nell’acqua. Oltre ai suoi effetti sugli organismi acquatici, le alte temperature dell’acqua possono aumentare la solubilità e quindi la tossicità di alcuni composti. Questi elementi includono metalli pesanti come cadmio, zinco e piombo, nonché composti come l’ammoniaca. La temperatura dell’acqua non solo può aumentare la solubilità dei composti tossici, ma può anche influenzare il limite di tolleranza di un organismo. I tassi di mortalità per lo zinco sono significativamente più elevati a temperature superiori a 25°C rispetto a temperature inferiori a 20°C. Questo si verifica perché la permeabilità dei tessuti, il tasso metabolico e il consumo di ossigeno aumentano con l’aumento della temperatura dell’acqua. In uno studio sul pesce Labeo bata, la concentrazione letale del 50% nelle 24 ore (LC50) a 15°C era di 540 mg/L, mentre a 30°C la LC50 è sceso a 210 mg/L.
L’ammoniaca è nota per la sua tossicità specialmente a livelli di pH elevati, ma la temperatura può anche influenzare le concentrazioni nella produzione consistente e costante. A basse temperature e a pH neutro, la seguente equazione rimane spostata a sinistra, producendo lo ione ammonio non tossico:
NH3 + H2O <=> NH4+ + OH–
Tuttavia, per ogni aumento di temperatura di 10°C, il rapporto tra ammoniaca non ionizzata e ammonio raddoppia. Nel 2013, l’EPA ha stabilito che la concentrazione massima media per le specie di acqua dolce è 17 mg/l di azoto ammoniacale totale (includendo sia NH3 che NH4+) a causa del suo potenziale salto di tossicità a pH e temperatura più elevati.
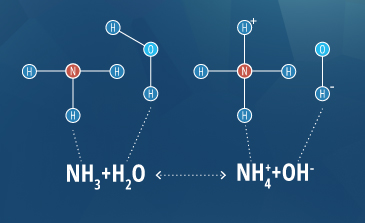
La temperatura dell’acqua può svolgere un ruolo nel passaggio tra ammonio e ammoniaca nell’acqua.
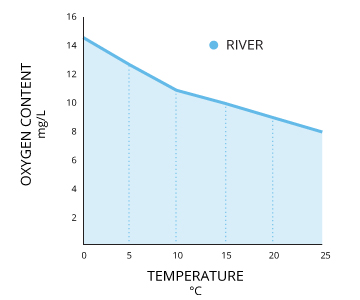
Le concentrazioni di ossigeno disciolto dipendono dalla temperatura. Più calda è l’acqua, meno ossigeno può trattenere.
Ossigeno disciolto e temperatura dell’acqua
La concentrazione di ossigeno disciolto dipende dalla temperatura. Più calda è l’acqua, meno ossigeno può trattenere. Ciò significa che nelle vasche o nei laghetti o nei bacini all’esterno più freddi possono contenere più ossigeno disciolto rispetto alle acque più calde degli acquari. Se l’acqua è troppo calda, non conterrà abbastanza ossigeno per la sopravvivenza degli organismi acquatici. Per questo spesso è importante per mantenere alti i livelli di ossigeno, far gorgogliare l’acqua o inserire un’areatore.

La temperatura regola numerose reazioni chimiche
La temperatura dell’acqua può influenzare la conducibilità in due modi. Poiché la conducibilità è misurata dal potenziale elettrico degli ioni in soluzione, è influenzata dalla concentrazione, carica e mobilità di quegli ioni. La temperatura dell’acqua influisce sulla viscosità, che a sua volta influisce sull’attività ionica e sulla conduttività. La mobilità ionica dipende dalla viscosità, che a sua volta dipende dalla temperatura. La viscosità si riferisce alla capacità di un liquido di resistere al flusso. Più è viscoso, meno è fluido; melassa e mercurio sono più viscosi dell’acqua. La relazione inversa tra temperatura e viscosità significa che un aumento della temperatura diminuirà la viscosità. Una diminuzione della viscosità dell’acqua aumenta la mobilità degli ioni nell’acqua. Pertanto, un aumento della temperatura aumenta quindi la conduttività. La conducibilità aumenta di circa il 2-3% per 1°C di aumento della temperatura, sebbene in acqua pura aumenterà di circa il 5% per 1°C. Questa variazione è il motivo per cui molti professionisti utilizzano un confronto standardizzato della conducibilità, noto come conduttanza specifica, che è corretto in temperatura a 25°C. Molti sali sono più solubili a temperature più elevate. Il secondo modo in cui la temperatura può influenzare la conduttività è attraverso la concentrazione ionica. Molti sali sono più solubili a temperature più elevate. Quando un sale si dissolve, si scompone nei suoi rispettivi ioni. Poiché l’acqua calda può dissolvere diversi minerali e sali più facilmente dell’acqua fredda, la concentrazione ionica è spesso più alta. L’aumento del contenuto di minerali e ioni può essere notato nelle sorgenti termali naturali, che promuovono le loro capacità di “guarigione”. Questi soluti disciolti sono spesso indicati come solidi disciolti totali o TDS. TDS si riferisce a tutte le particelle di ioni in soluzione che sono inferiori a 2 micron. Questi sali e minerali entrano nell’acqua dalle rocce e dai sedimenti a contatto con essa. Man mano che si dissolvono e la concentrazione ionica aumenta, aumenta anche la conduttività dell’acqua. La velocità con cui aumenta la conducibilità dipende dai sali presenti nella soluzione. La solubilità di KCl aumenterà da 28 g KCl/ 100 g H2O a 0°C a 56 g KCl/ 100 g H2O a 100°C, mentre la solubilità del solo NaCl aumenta da 35,6 g a 38,9 g NaCl/100 g H2O nello stesso intervallo di temperatura. Inoltre, ci sono alcuni sali che diventano meno solubili a temperature più calde e quindi influenzeranno negativamente la conduttività.
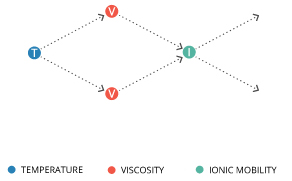
La temperatura dell’acqua influisce sulla viscosità, che a sua volta influisce sull’attività ionica e sulla conduttività.
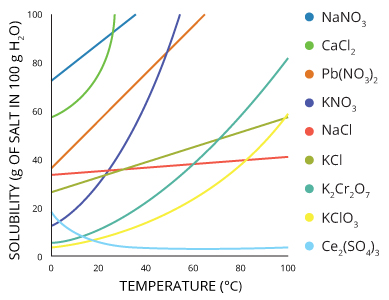
Molti sali sono più solubili a temperature più elevate.
Potenziale di riduzione dell’ossidazione e temperatura dell’acqua
Anche il potenziale di riduzione dell’ossidazione, noto come ORP, dipende dalla temperatura. L’effetto che la temperatura ha sui valori di ORP dipende dalle specie chimiche (atomi, molecole e ioni) presenti nella soluzione. I grafici di dipendenza dalla temperatura sono generalmente disponibili per le soluzioni di calibrazione, ma non per i campioni di campo.
Questa mancanza di dati è dovuta alla difficoltà di identificare e misurare ogni specie redoxing che potrebbe essere presente in una data fonte d’acqua. Poiché queste specie sono difficili da conoscere e definire quantitativamente negli studi ambientali, la maggior parte degli elettrodi ORP non compenserà automaticamente la temperatura. Tuttavia, la temperatura può ancora alterare una lettura e dovrebbe essere registrata con ogni misurazione considerata durante l’analisi dei dati
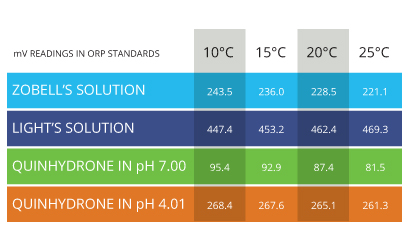
La temperatura dell’acqua influisce sull’ORP, ma in quale misura è difficile definire sul campo. I dati nelle soluzioni standard di calibrazione sono quantitativamente note e quindi è possibile misurare l’effetto della temperatura.
PH e temperatura dell’acqua
La temperatura dell’acqua può alterare il numero di ioni presenti, modificando il pH della soluzione senza renderla più acida o basica. Il pH è calcolato dal numero di ioni idrogeno in soluzione. A pH 7, gli ioni idrogeno e idrossile hanno concentrazioni uguali, 1 x 10-7 M, mantenendo la soluzione neutra. Tuttavia, queste concentrazioni sono vere solo a 25°C. Quando la temperatura aumenta o diminuisce, anche le concentrazioni di ioni si sposteranno, spostando così il valore del pH. Questa risposta è spiegata dal Principio di Le Chatelier. Qualsiasi modifica a un sistema in equilibrio, come l’aggiunta di un reagente o l’alterazione della temperatura, sposterà il sistema fino a raggiungere nuovamente l’equilibrio.
L’equazione:
H2O <=> H+ + OH–
è una reazione esotermica. Ciò significa che se la temperatura dell’acqua aumenta, l’equazione si sposterà a sinistra per raggiungere nuovamente l’equilibrio. Uno spostamento a sinistra diminuisce gli ioni nell’acqua, aumentando il pH. Allo stesso modo, se la temperatura dovesse diminuire, l’equazione si sposterebbe a destra, aumentando la concentrazione ionica e diminuendo il pH.
Il pH dell’acqua pura varia con la temperatura pur rimanendo perfettamente neutro rispetto al valore standard. L’acqua pura ha solo un pH di 7,0 a 25 gradi Celsius.
Tuttavia, ciò non significa che le variazioni di temperatura renderanno una soluzione più acida o basica. Poiché il rapporto tra idrogeno e ioni idrossile rimane lo stesso, l’acidità dell’acqua non cambia con la temperatura. Invece, l’intero intervallo di pH cambia, in modo che l’acqua neutra abbia un valore diverso da 7. L’acqua pura rimarrà neutra a 0 °C il pH è 7,47, a 25°C il pH è 7,00 e a 100°C il pH è 6,14.
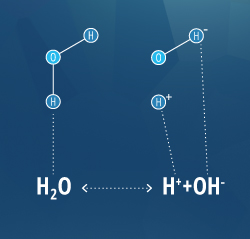
La temperatura dell’acqua può alterare il numero di ioni presenti,
modificando il pH della soluzione senza renderla più acida o basica.
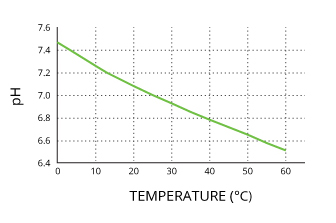
Il pH dell’acqua pura varia con la temperatura pur rimanendo perfettamente neutro.
L’acqua pura ha solo un pH di 7,0 a 25 gradi Celsius.
Densità e temperatura dell’acqua
La temperatura e la densità dell’acqua sono direttamente correlate. Quando la temperatura dell’acqua aumenta o diminuisce, altererà la densità dell’acqua. Questa è una relazione unica in quanto, a differenza della maggior parte dei materiali, la densità dell’acqua pura diminuisce di circa il 9% quando si congela 29. Questo è il motivo per cui il ghiaccio si espande e galleggia sull’acqua. L’acqua pura è anche unica in quanto raggiunge la sua densità massima, 1,00 g/ml, a 4°C. L’acqua a temperature superiori e inferiori a questa, compresa l’acqua surriscaldata e super raffreddata, galleggerà sull’acqua a 4°C.
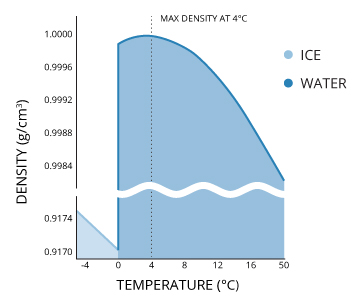
L’acqua è più densa a 4 gradi Celsius, ed è meno densa nella sua forma solida come ghiaccio.
Chiarimenti
Un semplice parametro come la temperatura può generare piccoli ma importanti cambiamenti degli equilibri biologici. È fondamentale tenerne conto specialmente in caso si allevano invertebrati, pesci o piante delicati o che hanno bisogno di particolari condizioni chimiche e fisiche. Spesso il risultato del buono sviluppo o della salute di un essere vivente può dipendere dalle condizioni di allevamento.
L’intero articolo è stato scritto per AqaZero.it; è vietata la riproduzione senza citare la fonte.